La découverte des antivitamines K (AVK) et leurs mécanismes découlent de deux étapes historiques pour le moins hasardeuses.
Dans les années 20 au nord des USA et au Canada, une hémorragie chez des bovins ayant consommé du trèfle de houx avarié fait rage.
Le dicoumarol est produit par le mélilot (trèfle doux, Melilotus sp.) sous l’action de champignons. On surnomma la maladie inconnue : « le mélilot gâté ».[10]
La warfarine ou coumadine est un dérivé de synthèse de la bishydroxycoumarine. Elle sera utilisée comme raticide.
A la fin des années 20 au Danemark, les biochimistes Henrick Dam et Schönheyder découvrent un trouble de l’hémostase (coagulation du sang) chez des poulets soumis à un régime strict en lipides dans le cadre d’une étude sur la synthèse du cholestérol.
La molécule incriminée dans ce trouble de la coagulation est huileuse, et l’administration de vitamines connues et/ou de lipides ne change pas l’état des poulets. Elle sera appelée vitamine K : K pour Koagulation en allemand.
En 1939, la formule chimique du phytoménadione ou alpha-phylloquinone par Dam et Almquis est découverte.[11]
Elle est synthétisée par E.Doisy et son équipe en 1941, on lui donne le nom de vitamine K1. Quelques années plus tard, Mckee et ses collègues synthétisent la vitamine K2. [11]
En 1951, une intoxication volontaire massive par un sujet avec de la warfarine, sans altération de son état clinique, incitera les scientifiques à son utilisation en thérapeutique.[10]
Ces anticoagulants oraux seront la seule classe thérapeutique utilisée à visée préventive et curative des pathologies thrombemboliques (pathologies provoquant une coagulation trop importante du sang) pendant des décennies.
Dans les années 2000, de nouvelles molécules voient le jour : les A.O.D, elles vont modifier les pratiques médicales.
On estime en France que 3,12 millions de patients en 2013 ont reçu au moins un anticoagulant toutes classes confondues.[3]
Du fait de leur action directe et spécifique, de leur faible contrainte de surveillance, d’une iatrogènie (pathologie induite par par le traitement lui-même…) moindre annoncée, les A.O.D suscitent dès lors beaucoup d’espoir et d’attente au sein des communautés internationales scientifique et médicale.
|
Coumariniques |
Dérivés de l’indanédione | |
|
Acénocoumarol |
Warfarine |
Fluindione |
| Sintrom®4 mg Minisintrom®1 mg |
Coumadine®(peu en France) 2 mg ou 5 mg |
Previscan® (très utilisé en France¹) 20 mg |
Les différents AVK commercialisés en France
Au Japon il existe aussi l’edoxaban (Lixiana®) ; le betrixaban est en phase d’étude II et III. [2]
|
Xabans |
Gatrans | |
|
Rivaroxaban : Xarelto® en 2008 |
Apixaban : Equilis® en 2012 |
Dabigatran étexilate : Pradaxa® en 2008 |
|
2,5 mg, 10 mg, 15 mg, 20 mg |
2,5 mg et 5 mg |
75 mg, 110 mg, 150 mg |
Les A.O.D commercialisés en France
Au Japon il existe aussi l’edoxaban (Lixiana®) ; le betrixaban est en phase d’étude II et III. [2]
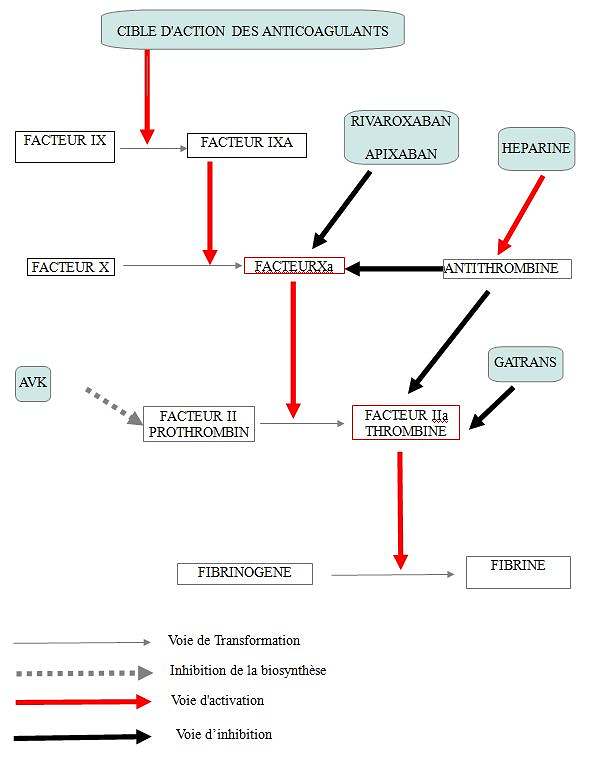
Points d’impact des différentes thérapeutiques (anticoagulants) citées ci-dessus
Consultons ensemble le tableau comparatif ci-dessous : A.O.D versus les AVK [2] ; [3]
Les informations décrites nous permettront de discuter des modalités de surveillance de ces thérapeutiques.
| Propriétés pharmacologiques |
AVK* |
Rivaroxaban |
Apixaban |
Dabigatran étexilate |
| Mode d’action | Inhibiteur des facteurs II, VII, IX, X | Inhibiteur direct du facteur Xa | Inhibiteur direct du facteur Xa | Inhibiteur direct du facteur IIa |
| Biodisponibilité |
100 % |
80 %-100 % |
80 % |
6,5 % |
| Pic d’action (t max) |
4-5 j |
1-3 h |
1-3 h |
1-3 h |
| Demi-vie (t1/2vie) |
36-42 H |
9-15 h |
9-13 h |
14-17 h |
| Voies de clairance |
Hépatique, rénale , digestive… |
65 % rénale |
25 % rénale |
80 % rénale |
| Cytrochrome |
Oui |
32 % |
15 % |
Non |
| Fixation protéique |
Oui |
95 % |
87 % |
35 % |
Tableau comparatif de la pharmacodynamie des A.O.D versus les AVK
Elle désigne le pourcentage du médicament administré qui parvient dans le compartiment central.
L’absorption du dabigatran dépend du pH gastrique : son action est diminuée en cas de traitement concomitant par inhibiteur de la pompe à protons.
L’efficacité clinique du dabigatran sera très variable et imprévisible selon les sujets compte tenu de la biodisponibilité extrêmement faible.
Le pic d’action est le temps que prend le médicament pour atteindre sa concentration sérique (sanguine) maximale.
T ½ La demi-vie est le temps requis que met le médicament à être éliminé de moitié de sa dose initiale dans la circulation sanguine. La demi-vie permet de mesurer l’élimination d’un médicament et permet de déterminer l’intervalle entre les doses.
La clairance est la fraction d’un volume théorique totalement épuré (c’est-à-dire ne contenant plus le médicament concerné) par unité de temps.
Les A.O.D sont contre-indiqués en cas de clairance de la créatinine inférieure à 15 ml/min (et de 30 ml/min pour le dabigatran), au-delà, les doses seront ajustées.
La fonction rénale devra être étudiée avant leur mise en route pour les populations âgées ou les populations à risque et elle sera surveillée au décours du traitement.
Pour les AVK, on sait que les interférences avec le métabolisme enzymatique (avec le cytochrome P450 2C9) réduisent leur efficacité lors de la coadministration d’inducteurs (rifampicine), ou au contraire augmentent le risque hémorragique lors de l’adjonction d’inhibiteurs (imidazolés, amiodarone, fluoroquinolones, antidépresseurs sérotoninergiques, millepertuis ou ritonavir).
De même, la compétition au niveau de la fixation protéique (fibrates) potentialisent les AVK et entraînent un risque plus ou moins important d’hémorragie.
Contrairement aux idées reçues, les A.O.D présentent eux aussi des interactions médicamenteuses selon leur profil pharmacodynamique au même titre que les AVK.
Le risque hémorragique peut être accru.
Il faut donc être vigilant lors de la prescription de ces thérapeutiques et lors du suivi.
On peut citer par exemple que les Gatrans sont contre-indiqués avec la plupart des antifongiques azolés et les médicaments de transplantation, qu’une surveillance étroite est recommandée avec la rifampicine et, que les Xabans et les Gatrans nécessitent une surveillance étroite avec les AINS (anti-inflammatoires non stéroïdiens) et certains antiarythmiques.
De nombreuses polémiques font rage depuis la mise sur le marché des A.O.D.[2]; [3]; [4]; [5]; [6]; [8]; [9]; [14];[15]; [16]
Il s’agit ici de vous présenter les études mondiales menées sur ces médicaments entre 2008 et 2014.
Ces analyses permettront de mieux guider les praticiens dans leurs prescriptions au vu des résultats révélés.
| Indication |
Dabigatran étexilate : Pradaxa® |
Rivaroxaban : Xarelto® |
Apixaban : Equilis® |
| Prévention de la MTEV
►Chirurgie de hanche ►Chirurgie du genou ►Médecine |
RE-NOVATE 2
RE-NOVATE 2 RE-MODEL(EU) RE-MOBILIZE(US) |
RECORD-1
RECORD-2 RECORD-3(EU*) RECORD-4(US*) MAGELLAN |
ADVANCE-1
(vs enoxaparine) ADVANCE-2 ADVANCE-2(EU*) APROPOS(US*) ADOPT |
| Embolie pulmonaire | EINSTEIN-PE | ||
| Prévention de la TVP aiguë > 6 mois | RECOVER-1
RECOVER-2 |
EINSTEIN-DVT | AMPLIFY |
| Prévention de la TVP chronique > 6mois | REMEDY(vs AVK)
RE-SONATE(vs Pl*) |
EINSTEIN-EXT | AMPLIFY-EXTENSION |
| FA non valvulaire | RE-LY | ROCKET-AF
J-ROCKET-AF |
ARISTOTLE
AVERROES(vs Pl*) |
| SCA* | RE-DEEM | ATLAS CAS-TIMI51 | APPRAISE |
Les études cliniques et les indications
SCA= Syndrome Coronarien Aigu
Pl= Placebo
EU= Europe
US= Etats-Unis
Les facteurs d’exclusion de ces méta analayses sont :
Les avantages de ces études sont :
Les résultats de ces études ont montré que le risque hémorragique n’est pas inférieur à celui des autres anticoagulants (héparines, AVK).[2];[7]; [8]; [9]; [12]; [14]; [15]; [16]; [17]
Leur praticité d’usage au quotidien, leur brève demi-vie, leur action rapide et une absorption facile sont des arguments valables qui peuvent inciter à la prescription des A.O.D, si en plus on prend en compte le coût financier moins onéreux de ces thérapeutiques, on peut y voir un avantage sociétal non négligeable.
Quelques réflexions s’imposent, les essais cliniques ont été réalisés en double aveugle avec des cohortes estimables mais les critères d’exclusion cités ci-dessus sont nombreux :
Devant un IMC faible, une polymédication ou des comorbidités associées, chez les sujets âgés, les insuffisants rénaux mêmes modérés, il est préférable d’instaurer une surveillance faute d’études et donc de recul, ce d’autant qu’il n’ existe pas d’antidote.
Dans la maladie thromboembolique et l’embolie pulmonaire les études RE-COVER1/2 puis par extension RE-MEDY, RE-SONATE, RE-LY cf tableau, sont intéressantes.[12]; [16]; [17]
Il s’agit d’une analyse de cohorte randomisée en double aveugle qui compare des patients après une durée médiane de 9 jours d’un traitement parentéral anticoagulant dans les deux bras puis sous dabigatran à la dose de 150 mg X 2 / j (+ placebo de warfarine) AVK (+placebo de dabigatran) avec un objectif cible INR (2-3) pendant 6 mois. [12]
Le critère principal de jugement de l’étude RE-COVER était l’incidence à 6 mois d’une récidive symptomatique confirmée de TVP et les décès reliés.
Le dabigatran est non inférieur aux AVK sur le critère primaire : récidives de thromboses symptomatiques documentées, létales ou non. [16]; [17]
Il a été observé 2,4 % de récidives dans le groupe dabigatran versus 2,1 % dans le groupe warfarine. Des saignements majeurs ont été notés chez 1,6 % des patients du groupe dabigatran vs 1,9 % dans le groupe warfarine (hazard ratio dabigatran 0,71 IC 95 % 0,59-0,85), les seules hémorragies tendant à être augmentées sous dabigatran sont les hémorragies gastro-intestinales dont la raison n’est pas encore élucidée (non-respect du schéma d’administration ; pathologie gastro-intestinale sous jacente ; concomitance alimentaire ?) et pas de différence en termes de mortalité.[16]; [17]
Les essais plus récents confortent ces résultats, ceci constitue une petite révolution dans la prise en charge de la maladie TVP et de l’embolie pulmonaire compte-tenu de la praticité de la molécule au quotidien et d’une moindre surveillance.[5]; [7]; [9]; [16]; [17]
A ce jour, les consensus internationaux considèrent que les A.O.D sont une alternative aux héparines de bas poids moléculaire et aux AVK, et constituent un progrès dans la prévention de la maladie thrombo-embolique en chirurgie chez le sujet jeune observant, sans facteur de risque.
On retiendra qu’après une prothèse du genou, la durée de traitement recommandée est de 10 à 14 jours et après prothèse de hanche, elle est de 32 à 38 jours. [2]; [3]; [8]
Ce qu’il faut retenir
Avantages des A.O.D par rapport aux AVK dans la FANV et prévention des complications secondaires énoncée dans ce tableau : [2];[3];4]
| Accident vasculaire cérébral(AVC) ou embolie systémique(ES) | Hémorragies intracrâniennes | Hémorragies majeures | Mortalité globale | |
| Apixaban :
Equilis®5mgX2/j |
↓ |
↓ |
↓ |
↓ |
| Dabigatran étexilate :
Pradaxa® 110 mg |
═ |
↓ |
═ |
═ |
| Dabigatran étexilate :
Pradaxa® 150 mg |
↓ |
↓ |
═ |
═ |
| Rivaroxaban :
Xarelto® 15/20 mg |
NA |
↓ |
═ |
═ |
Avantages des A.O.D par rapport aux AVK dans la FANV et prévention des complications secondaires
Selon les résultats de ces essais cliniques, l’apixaban a une efficacité sensiblement supérieure à la warfarine pour la prévention des AVC et des ES, pour la mortalité globale et peut-être les complications hémorragiques.[2]
Le dabigatran et le rivaroxaban n’ont pas formellement démontré d’avantage par rapport aux AVK, malgré une probable réduction somme toute modeste du risque hémorragique intracrânien.
Il faut rappeler que les A.O.D sont à ce jour contre-indiqués en cas de prothèse valvulaire. L’essai clinique RE-ALIG qui a étudié le dabigatran versus warfarine chez des patients porteurs de prothèse valvulaire cardiaque nécessitant un traitement anticoagulant, observe une mortalité augmentée.[2]; [3]; [6]
Le maniement des A.O.D nécessite du recul et incite à la prudence tout comme avec les AVK* mais pour des raisons différentes :
En 2006, on se souvient du retrait du marché pour risque hépatique du ximelagatran/mélagatran, qui avait eu pourtant l’AMM en 2003 ; un risque coronarien avait même été évoqué à cette époque.
Il faut donc être vigilant.
Les AVK restent dans la prévention des AVC et des ES chez les patients présentant une FANV, la recommandation consensuelle.
Les A.O.D méritent considération chez des patients plutôt jeunes, observants, non polymédicamentés et sans facteurs de risque avérés comme la dénutrition, l’insuffisance rénale chronique et/ou hépatique.
Passer des AVK à ces molécules ne présente aucun intérêt, surtout si ils sont bien tolérés et bien contrôlés. Ce pourrait même être délétère compte tenu de l’absence de contrôle de l’efficacité de ces dernières au quotidien et de la difficulté clinique et intellectuelle du passage de l’un à l’autre.[2];[3]
Néanmoins, chez des patients atteints de FANV avec des facteurs de risque aux AVK, les autorités françaises de santé ont rappelé qu’une prescription des A.O.D est défendable :
La perspective de tests de surveillance et d’antidotes possibles permettront, dans un futur espéré proche, à ces A.O.D d’être une alternative.
Ce qu’il faut retenir
Le traitement antithrombotique pour la prévention secondaire des événements ischémiques à la suite d’un syndrome coronarien aigu (SCA) repose selon les recommandations sur l’utilisation conjointe d’un antiagrégant plaquettaire et du clopidogrel ou prasugrel.[2]
On sait que le risque d’un nouvel accident thrombotique, même après un geste de revascularisation, persiste en partie à cause d’une production prolongée de thrombine.
Des essais cliniques ont testé les A.O.D dans cette situation précise.
En conclusion, chez les patients récemment atteints d’un SCA, l’association d’un A.O.D au traitement antiplaquettaire est insatisfaisante.
Elle ne réduit pas sensiblement le risque ischémique, elle augmente même de manière significative le risque hémorragique, surtout lors de l’adjonction aux deux agents antiagrégants plaquettaires.
Les recommandations scientifiques actuelles ne préconisent pas l’ajout d’un anticoagulant.
Ce qu’il faut retenir
Lors de la préparation de ce sujet, je souhaite porter à l’attention du lecteur la révélation d’un effet indésirable possible secondaire à la prise du dabigatran en particulier.[13]
Je cite en référence un article paru sur le web : qui s’intitule « Sur-risque d’infarctus sous Pradaxa : un effet classe des anti-IIa ? »
En résumé : « il y aurait plus d’infarctus avec les inhibiteurs oraux directs de la thrombine et en particulier le dabigatran à la posologie de 150 mg X 2/j mais pas moins d’IDM avec la warfarine avec la double conclusion qui est celle d’un sur-risque d’événements ischémiques, et non d’un effet protecteur de la warfarine, et d’un sur-risque que les auteurs estiment « probablement lié à la classe thérapeutique elle-même ». Les auteurs assènent qu’il est impératif que dans les futures études d’antithrombotiques, quelles que soient leurs classes, des données claires, non équivoques et dégroupées, soient publiées sur la totalité des évènements thromboemboliques indésirables, y compris les IDM, et ceci, à tous les stades du développement ».
Des méta-analyses doivent être menées sur ce thème, en attendant, une surveillance doit rester la norme quant à la survenue d’un tel événement.
Ce qu’il faut retenir
Sur-risque d’infarctus sous Dabigatran : un effet classe des anti-IIa ? : question ouverte, meta-analyses en attente, en attendant, la vigilance doit être de mise.
Je me propose de vous référencer dans ce tableau, les indications recommandées et possibles des A.O.D en conformité avec les résultats issus des méta-analayses.
| Indications |
Dabigatran étexilate : Pradaxa® |
Rivaroxaban : Xarelto® |
Apixaban : Equilis® | ||||
|
75/110 mg |
110/150 mg |
2,5 mg |
10 mg |
15/20 mg |
2,5 mg |
2,5/5 mg | |
| Prévention des ETEV* dans une chirurgie de hanche ou de genou programmée, | Oui | Oui | Oui | ||||
| Prévention des AVC* et ES* chez des sujets atteints d’une FAVN* avec 1 ou +FDR*, | Oui | Oui | Oui | ||||
| Prévention des événements athérothrombotiques post-SCA* avec enzymes cardiaques élevées, | Oui
Avec un ou des antiagrégants plaquettaires | ||||||
| Traitement des TVP* et prévention des récidives de TVP* et EP* post TVP* aiguë. | Oui |
Indications recommandées et possibles des A.O.D en conformité avec les résultats issus des méta-analyses
ETEV = événement thrombo-embolique veineux,
AVC = accident vasculaire cérébral,
ES = embolie systémique,
FAVN = fibrillation atriale non valvulaire,
FDR = facteur de risque,
SCA = syndrome coronarien aigu,
TVP = thrombembolie veineuse,
EP = embolie pulmonaire.
Les A.O.D à ce jour, constituent un outil thérapeutique novateur et alternatif aux thérapeutiques usuelles dans quelques indications.
Les études ont démontré une efficacité au moins équivalente aux AVK notamment dans la prévention de la maladie thrombo-embolique.
Leur coût financier faible, leur praticité d’usage et certains avantages pharmacodynamiques ont été reconnus et validés par les hautes autorités sanitaires françaises, on parle de SMR (service médical rendu).
Mais l’absence d’antidotes et de tests fiables qui évaluent l’efficacité des A.O.D, sont des inconvénients non négligeables.
Les praticiens devront prendre en compte comme toujours, les facteurs de risque du patient comme l’âge, les antécédents médico-chirurgicaux et les médications en cours au moment de l’instauration de la prescription, afin d’appréhender les bénéfices/risques opposables.
La mesure de la clairance de la créatinine est nécessaire à l’introduction du traitement mais aussi dans le suivi, chez les sujets âgés.
Les posologies et les schémas d’administration doivent être connus par les professionnels de santé et enseignés aux patients afin de favoriser l’observance tout comme avec les AVK.
Enfin, le bon sens préconise de ne pas modifier un traitement qui fonctionne, si le patient sous AVK est correctement équilibré avec une tolérance satisfaisante, il est inutile voire dangereux de se hasarder à un changement.
A ce jour la révolution n’a pas eu lieu mais les progrès sont notables. Ces thérapeutiques viennent en complément de l’arsenal médicamenteux connu.
Les A.O.D sont des molécules prometteuses sous réserve dans le futur d’antidotes et de tests de surveillance adéquats.
Image par PublicDomainPictures de Pixabay
1 Allain Pierre :Nouveaux anticoagulants, dabigatran, rivaroxaban, apixaban. Pharmacorama, 2011;1.
2 www.academie-medecine.fr Rapport sur les anticoagulants oraux directs (AOD)
(antérieurement appelés « nouveaux anticoagulants oraux » ou NACO), 10 juin 2014.
3 www.ansm.sante.fr Les anticoagulants en France en 2014: état des lieux, synthèse et surveillance.
4 Becattinicet al.Old and new oral anticoagulants for venous thromboembolism and atrial fibrillation: a review of the literature. Thomb Res,2012; 129: 392-4002.
5 BulleRhRet al.for The EINSTEIN-PE Investigators. Oral rivaroxaban for the treatment of symptomatic pulmonary embolism. N Engl J Med, 2012; 366: 1287-1297.03.
6 Connoly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, Pogue J, Reilly PA, Themeles E, Varrone , Wang S, Alings M, Xavi D, Zhu J, Diaz R, Lewis BS, Darius H, Dienerhc, Joyner CD, Wallentin L; RE-LY Steering Comittee and Investigators Dabigatran versus warfarin in patients with atrial fibrillation [published correction appears in N Engl J Med
2010;363:1877 N Engl J Med2009; 36: 1139-51.
7 D.Delsart, P.MisMetti. Les nouveaux anticoagulants oraux s’attaquent à l’embolie pulmonaire. Réalités Cardiologiques, 2012 ; 288: 33-37.
8 Eriksson B. I., Dahl O. E., Rosencher N. et al. Oral dabigatran etexilate vs subcutaneous enoxaparin for the prevention of venous thromboembolism after total knee replacement: the RE-MODEL randomized trial, Journal of Thrombosis and Haemostasis 2007, 11, 2178-85
9 Eriksson B. I., Dahl O. E., Rosencher N. et al. Dabigatran etexilate vs enoxaparin for prevention of venous thromboembolismafter total hip replacement : a randomised double blind non inferiority trial Lancet2007, 370,2004-7
10 Fellalo Fulu Pumi Kennel Joel Kuhlmann Dossier Toxicologie Mars 2011, 1ere édition.
12 www.medscape.fr/voirarticle/3032451: Le dabigatran fait ses preuves face aux AVK dans la thrombose veineuse profonde: Solère Pascale 08 décembre 2009.
13 www.medscape.fr/voirarticle/3591407: Sur-risque d’infarctus sous Pradaxa : un effet classe des anti-IIa?: Bargoin Vincent 24 octobre 2013.
14 The VanghoghInvestigators. Idraparinux versus standard therapy for venous thromboembolic disease. N Engl J Med,2007; 357: 1094-1104.04.
15 The Einstein Investigators. Oral rivaroxaban for the treatment of symptomatic venous thromboembolism. N Engl J Med,2010; 363: 2499-510.05.
16 Schulman S, Eriksson H, Goldhaber SZ et coll. Dabigatran exilate versus warfarine in the treatment of venous trhromboembolism. Session plénière, ASH, 6 décembre 2009.
17 Schulman S, Kearon C, Kakkar AK et coll. Dabigatran versus warfarine in the treatment of acute venous thromboembolism. NEJM2009; 361 (24): 2342-52.